|
Die Mundhöhle verbindet die Außenwelt mit sensiblen Organsystemen wie dem Resiprations- und Verdauungstrakt und ist damit eine unmittelbare Eintrittspforte für Infektionserreger wie das SARS-Cov-2-Virus.
Inwieweit chronisch entzündliche Läsionen oraler Gewebe wie Gingivitis, Parodontitis, aber auch Mukositis und Sialadenitis Auswirkungen auf den Verlauf und Schweregrad einer Covid-19-Erkrankung haben und zum Auftreten von Komorbiditäten beitragen, war und ist Gegenstand zahlreicher aktueller Untersuchungen. Auch wenn noch viele Fragen geklärt werden müssen, so gibt es doch bereits deutliche Hinweise auf derartige Zusammenhänge.
Rezeptorproteine der oralen Gewebe begünstigen die Infektion
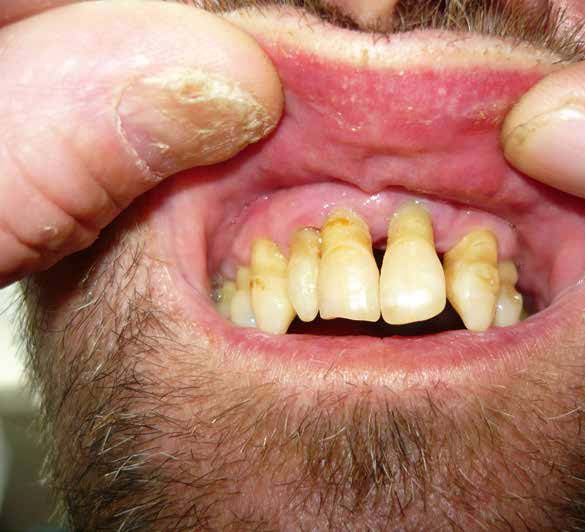
Zellen der Speicheldrüsen, der Mundschleimhaut und des Zahnfleisches exprimieren eine hohe Anzahl von ACE-2-Rezeptoren, welche die wichtigsten Membranstrukturen für das Andocken und Eindringen des Virus darstellen. Vor allem der gingivale Sulkus ist eine potenzielle Nische für SARS-Cov-2. Es ist bekannt, dass sich, besonders im Falle einer floriden Parodontitis, in den Biofilmen der tiefen Zahnfleischtaschen neben atypischen, nichtoralen Bakterien auch Viren ansiedeln. So stehen Erreger wie das Cytomegalievirus (CMV), das Epstein-Barr-Virus (EBV) und das Herpes simplex-Virus (HSV) in einer Art symbiontischen Wechselbeziehung zu der bakteriell-fungalen Biozönose. Ähnliche Mechanismen benützt auch das SARS-Cov-2-Virus. Dabei stellt sich natürlich die Frage, ob es sich nur passager und kurzfristig im Sulkus befindet oder ob es dort persistiert und die Zahnfleischtaschen damit zu einem Dauerreservoir und einem gefährlichen infektiösen Streuherd werden.
Parodontitis – ein Risikofaktor für die Covid-Erkrankung
Eine Studie an 568 Patienten hat gezeigt, dass der oralen Mukosa eine wichtige Rolle bei der Transmission und Pathogenität von SARS-Cov-2 zukommt und dass chronische Entzündungen des Zahnhalteapparats ein unabhängiger Risikofaktor für die Schwere des Verlaufs einer Covid-Erkrankung sind. Die American Academy of Periodontology postuliert ein gegenüber parodontal Gesunden signifikant erhöhtes Risiko für Komplikationen einer Covid-Infektion bei gleichzeitigem Vorliegen einer moderaten bis schweren Parodontitis. Die Zahl der Patienten, welche einer Intensivpflege oder sogar einer künstlichen Beatmung bedurften, war gegenüber einer parodontal gesunden Vergleichsgruppe um das Dreifache erhöht. Covid-Kranke mit florider Parodontitis zeigten deutlich höhere Level von mit bekanntlich schlechtem Outcome assoziierten Biomarkern, wie D-Dimer und C-reaktivem Protein. Umgekehrt führt die Covid-2-Infektion auch zur Progression einer vorbestehenden Parodontitis.
Wechselwirkungen zwischen SARS-Cov-2 und dem oralen Mikrobiom
Die Ursachen für diese fatale Wechselbeziehung sind vielfältig. Die Integration des Virus in das orale Mikrobiom führt vermutlich zu einer Veränderung des Mundhöhlenmilieus. Damit kommt es zu einer Dysbiose, welche mit einer Artenverarmung und einem Überhandnehmen potenziell pathogener Bakterien einhergeht. Dies verstärkt einerseits die parodontale Entzündung, beeinflusst aber auch durch systemische Dissemination der beteiligten Keime die Gesamtgesundheit. Die Bakterien aus den Zahnfleischtaschen werden über Aspiration, Verschlucken und durch bakteriämische Aussaat fast im gesamten Körper verbreitet. Orale Bakterien aus subgingivalen Biofilmen wie etwa Porphyromonas gingivalis, Prevotella intermedia, Fusobacterium nucleatum und Aggregatibacter actinomycetem comitans verändern ihrerseits die Umweltbedingungen in Darm und Bronchien und schaffen eine entzündungsaffine Umgebung. Sie induzieren, obwohl selbst oft nur in geringer Menge vorhanden, als sogenannte „Keystone“- Bakterien eine pathologische Veränderung der ortsständigen Mikrobiome und machen die Gewebe für chronisch entzündliche Erkrankungen anfällig – und sogar für Dysplasie und Karzinomentstehung. Auf diesem Weg etablieren die bakteriellen Erreger ein inflammatorisches Netzwerk mit Sars-Cov-2. Sie induzieren durch die von ihnen hervorgerufene Entzündung sowohl in der Mundhöhle als auch in den tiefen Atemwegen und im Gastrointestinaltrakt eine stark vermehrte Expression von ACE-2-Rezeptoren auf den Zellmembranen und fördern die Bildung von Endopeptidasen. Sie schaffen so ideale Voraussetzungen für das Eindringen des Coronavirus in sensible Strukturen. Diese einander verstärkenden Pathomechanismen gefährden besonders Patienten mit vorbestehenden Komorbiditäten wie Diabetes mellitus, Immunschwäche oder konsumierenden Allgemeinerkrankungen. Möglicherweise – hier liegen noch keine eindeutigen Ergebnisse vor – erhöhen die Parodontitiskeime zusätzlich die Virulenz des Virus durch Spaltung des S-Glykoproteins. Bei der Immunreaktion gegen parodontal-pathogene Bakterien werden vermehrte TH17-Lymphozyten gebildet. Dabei handelt es sich um einen speziellen Typ von T-Helferzellen, welche eine wichtige Rolle bei der Aktivierung der neutrophilen Granulozyten spielen. Über diese Schiene wird in der Folge der bei Covid-19-Infektionen so gefürchtete Zytokinsturm gefördert und verstärkt. Wenn auch noch viele Fragen über die komplexen Mechanismen im Zusammenspiel zwischen oralen Keimen und dem Coronavirus offen sind, so kann man auf Grund der vorhandenen Daten doch davon ausgehen, dass der parodontale Status und die orale Gesundheit einen wichtigen Faktor für Schwere und Verlauf einer Covid-19-Infektion darstellen. Gerade in der Zeit der Pandemie dürfen Mundhygiene, regelmäßige zahnärztliche Kotrollen und frühzeitige Intervention zur Vermeidung aufflammender Entzündungen nicht vernachlässigt oder hintangestellt werden. Wie bei vielen anderen interdisziplinären medizinischen Fragestellungen erweist sich auch bei der Covid-19-Krankheit die Mundhöhle als Drehscheibe der Gesamtgesundheit.
DDr. CHRISTA EDER
FA für Pathologie und Mikrobiologin
eder.gasometer@chello.at
|